Liệu pháp tế bào NK cho các khối u não
Khối u não là sự phát triển của những mô trong não hoặc xung quanh não. Sự phát triển này liên quan đến nhu mô não và những khu vực xung quanh. Những vị trí xung quanh này bao gồm các dây thần kinh, tuyến yên, và những lớp màng bọc bề mặt của não bộ. Có hai loại u não chính được xác định dựa trên sự tác động của khối u lên cơ thể là khối u não lành và khối u não ác tính (ung thư). Trong quá trình u não phát triển lan vào não từ những phần khác của cơ thể. Những khối u này là ung thư não thứ cấp và thường được gọi là ung thư não di căn. Các khối u não lành tính thường là khó phát hiện ra các triệu chứng và được cho là có sự phát triển chậm hơn u não ác tính. Chúng có thể gây ra các triệu chứng tinh vi mà ban đầu khó nhận thấy. Các triệu chứng có thể trở nên tồi tệ hơn trong nhiều tháng hoặc nhiều năm. Các khối u não ác tính gây ra các triệu chứng rõ rệt hơn. Đa số các triệu chứng xảy ra đột ngột và trở nên tồi tệ hơn trong vài ngày hoặc vài tuần. Từ đó có thể dẫn tới tử vong, chính vì vậy chúng ta cần can thiệp và dự phòng sớm cho mặt bệnh này. Liệu pháp tế bào NK đã đem đến cho chúng ta một lựa chọn với tiềm năng đáp ứng trong quá trình điều trị bệnh u não.
TẢI FILE PDF TẠI ĐÂY: Liệu pháp tế bào NK cho các khối u não – PDF
1. Nguyên nhân và đặc điểm của bệnh
Một thống kê của Mỹ vào năm 2023, ước tính có khoảng 24.810 người trưởng thành và 5.230 trẻ em dưới 20 tuổi được chẩn đoán mắc các khối u ung thư nguyên phát ở não. Trên toàn thế giới, ước tính có khoảng 308.102 người được chẩn đoán mắc khối u nguyên phát ở não hoặc tủy sống vào năm 2020. Ung thư não và các hệ thống thần kinh khác là nguyên nhân gây tử vong đứng thứ 10 khi ước tính khoảng 18.990 trường hợp tử vong do ung thư não và thần kinh trung ương vào năm 2023 [1]. Khởi đầu bằng những khối u nguyên phát ngay trong não hoặc trong mô gần đó. Lý do là các tế bào trong hoặc gần não có những thay đổi trong DNA của chúng. Những thay đổi này làm tế bào phát triển nhanh và sức sống mạnh mẽ trong khi các tế bào khỏe mạnh sẽ chết đi như một phần của tự nhiên. Điều này tạo ra rất nhiều tế bào phụ dư thừa trong não, từ đó hình thành khối u [2]. Với nhiều người bị u não, nguyên nhân vẫn chưa được hiểu rõ. Đôi khi, cha mẹ chuyển DNA bị đột biến cho con. Những thay đổi có thể làm tăng nguy cơ bị u não nhưng sự di truyền này rất hiếm. Khi khối u não xảy ra ở trẻ em, chúng có khả năng là khối u não nguyên phát. Ở người lớn, khối u não có nhiều khả năng là ung thư của một cơ quan khác và di căn đến não. Có một số yếu tố có thể gây ra khối u não như tuổi, tần suất tiếp xúc bức xạ, các hội chứng di truyền [2].
Những tiến bộ trong điều trị hóa trị, xạ trị và các thủ thuật phẫu thuật thần kinh đã làm tăng khả năng sống sót của bệnh nhân bị u não. Tuy nhiên, các khối u ác tính như u thần kinh đệm cấp độ cao, u nguyên bào tủy và u thần kinh đệm cầu não lan tỏa mang lại kết quả không mong muốn do tái phát hoặc tiến triển [3]. Bất chấp các phác đồ mang lại hiệu quả điều trị tích cực bao gồm phẫu thuật, xạ trị và hóa trị nhưng nhiều khối u hệ thần kinh trung ương vẫn không thể chữa khỏi. Do tính không đồng nhất trong khối u và khả năng của các tế bào trốn tránh miễn dịch và ngăn chặn khả năng miễn dịch chống khối u là một số hạn chế có ảnh hưởng lớn [3]. Một hạn chế chính khác ảnh hưởng đến hiệu quả của liệu pháp điều trị chính là hàng rào máu não gây ra sự ngăn chặn các phân tử hoặc thuốc hướng đích và một số tác dụng phụ lên toàn cơ thể. Tuy nhiên, các nghiên cứu tiền lâm sàng trong thập kỷ qua đã thay đổi nhận thức này và cho thấy vai trò quan trọng của các tế bào miễn dịch trong khối u não [4]. Bên cạnh các tế bào ung thư ác tính chính, xung quanh khối u còn bao gồm nhiều loại tế bào khác nhau tạo thành vi môi trường khối u. Người ta nhận thấy rằng một số các loại tế bào lân cận trong vi môi trường này có vài trò điều hòa mạnh mẽ các yếu tố tác động đến khối u như phát triển hay ức chế [5].
2. Tế bào NK và cơ chế hoạt động trong bệnh u não
Tế bào giết tự nhiên (NK) là các tế bào lympho dạng hạt lớn đóng vai trò quan trọng trong khả năng miễn dịch chống ung thư. Khi kích hoạt, các tế bào NK gây ra quá trình chết theo chương trình của tế bào đích thông qua khả năng gây độc tế bào phụ thuộc vào tiếp xúc chủ yếu qua trung gian perforin và granzyme và bài tiết các cytokine tiền viêm như yếu tố hoại tử khối u-α và interferon-γ. Trong các khối u não, các tế bào NK đã được chứng minh là có hiệu quả trong ống nghiệm và in vivo [6]. Chúng có thể nhận biết và tiêu diệt các tế bào u nguyên bào thần kinh đệm ở người biểu hiện các đặc tính giống như tế bào gốc.
Các tế bào NK tạo thành một phần không thể thiếu của quần thể tế bào miễn dịch trong khối u trong môi trường vi mô khối u não. Nhiều nghiên cứu đã điều tra số lượng và hoạt động của tế bào NK ở những bệnh nhân bị u não. Các tế bào NK có mặt trong các khối u não di căn vào u sọ và thường xâm nhập vào u nguyên bào thần kinh đệm [7]. Các phương pháp để tăng cường chức năng chống khối u của tế bào NK bao gồm kích hoạt phản ứng phá hủy DNA (DDR) để tạo ra các phối tử nhằm kích hoạt các thụ thể của tế bào NK. Chất ức chế proteasome bortezomib (BTZ) kích hoạt DDR và làm cảm ứng các tế bào GBM để tế bào NK tiêu diệt bằng cách tạo các phối tử kích hoạt thụ thể NKG2D và DNAM-1. Điều trị BTZ với các tế bào NK tự thân đã ức chế sự phát triển của khối u và kéo dài thời gian sống sót ở 25% động vật thử nghiệm. Tuy nhiên, thiết lập BTZ phù hợp với tế bào NK vẫn được tối ưu hóa [6].
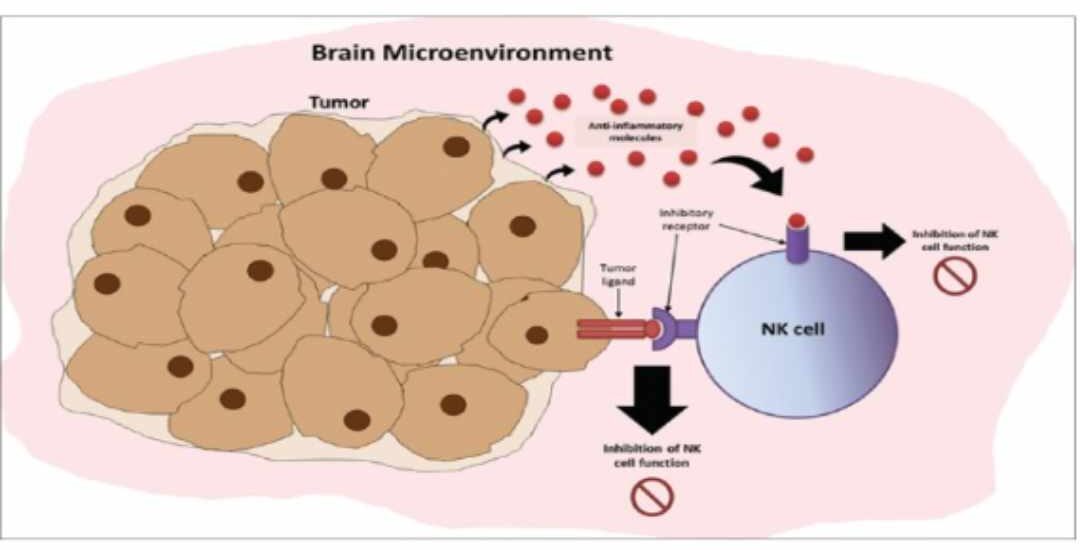
Hoạt động của tế bào NK ở bệnh nhân bị u não thường là kém do các yếu tố ức chế miễn dịch được giải phóng bởi các tế bào khối u (Hình 1). Ví dụ, các tế bào u thần kinh đệm biểu hiện dạng đặc biệt của MHC-I, hoạt động ức chế biểu hiện trên tế bào NK.
Hình 1: Các cơ chế trốn tránh miễn dịch của các khối u não chống lại sự giám sát và tiêu diệt tế bào giết người tự nhiên (NK) trong môi trường vi mô não [7].
Böttcher và cộng sự [8] đã báo cáo rằng các khối u tiết ra các chất trung gian gây viêm như cyclooxygenase và prostaglandin E2 ngăn chặn hoạt động chống ung thư của tế bào NK. Ở những bệnh nhân bị u nguyên bào thần kinh đệm đa năng, Fadul và cộng sự [9] đã thấy tế bào NK giảm đi trong mẫu khối u bị cô lập sau điều trị bằng bức xạ và temozolomide. Số lượng NK và hoạt động gây độc tế bào đã được điều hòa quá mức do các phân tử chống viêm, như yếu tố tăng trưởng biến đổi-β (TGF-β). Thách thức lớn đối với các liệu pháp tế bào NK trong ung thư thần kinh là môi trường ức chế miễn dịch của các khối u não có thể làm ức chế tế bào. Tuy nhiên, liệu pháp miễn dịch áp dụng cho các khối u não bằng tế bào NK hứa hẹn nếu chúng được kích hoạt và mở rộng ex vivo và sau đó được tiêm vào khối u sau khi cắt bỏ [7].
3. Nghiên cứu lâm sàng
Các tế bào NK có thể đóng một vai trò quan trọng trong các phản ứng miễn dịch chống khối u ở những bệnh nhân mắc các khối u não khác nhau. Castriconi và cộng sự [10] đã chỉ ra rằng các tế bào NK có thể tiêu diệt các tế bào u nguyên bào thần kinh đệm ở người biểu hiện các đặc tính giống như tế bào gốc. Ishikawa và cộng sự [11] đã chứng minh rằng các tế bào NK tự thân là an toàn và có hiệu quả một phần ở những bệnh nhân bị u thần kinh đệm ác tính tái phát ghi nhận ở 4 trong số 9 bệnh nhân. Hiệu quả một phần của các tế bào NK có thể là do cơ chế ức chế miễn dịch khối u gây ra và cơ chế trốn miễn dịch. Một số thử nghiệm giai đoạn đầu đang nghiên cứu liều lượng, độ an toàn và tác dụng phụ của liệu pháp tế bào NK trong điều trị ung thư tiến triển.
Trong các khối u não ở trẻ em, các tế bào NK có hiệu quả đối với u nguyên bào tủy. Một thử nghiệm lâm sàng giai đoạn 1 hiện đang được tiến hành, các tế bào NK mở rộng tự thân được tiêm vào não của những bệnh nhân đã trải qua phẫu thuật cắt bỏ các khối u dưới tái phát. Các thử nghiệm lâm sàng giai đoạn 2 đang sử dụng các tế bào NK tự thân mở rộng kết hợp với các tế bào T để tấn công các khối u não ở trẻ em có nguy cơ cao. Người ta tin rằng các liệu pháp kết hợp liên quan đến tế bào NK có thể nâng cao hiệu quả và/hoặc vượt qua các cơ chế trốn thoát miễn dịch của khối u não [7]. Mặc dù các thử nghiệm giai đoạn đầu này rất quan trọng để nhận ra liều lượng, độ an toàn và hiệu quả tối ưu của các liệu pháp tế bào NK, nhưng các quy trình kết hợp có thể là bắt buộc để thu được đầy đủ lợi ích của liệu pháp tế bào nuôi dưỡng. Ngoài ra, liệu pháp này còn có thể tạo ra các phản ứng miễn dịch như đào thải ghép vật chủ GvDH, chi phí mở rộng tế bào NK rất tốn kém và gồm nhiều bước [12].
Nói chung, các tế bào NK đóng một vai trò quan trọng trong khả năng miễn dịch chống khối u và đã được chứng minh là có mặt trong các cơ sở khối u não. Các nghiên cứu lâm sàng và tiền lâm sàng ban đầu dựa trên các liệu pháp tế bào NK tự thân chống lại các khối u não đã cho thấy một số hứa hẹn. Các thử nghiệm và nghiên cứu sâu hơn là cần thiết để làm sáng tỏ thêm các cơ chế mà qua đó các tế bào khối u trốn tránh sự giám sát và tấn công qua trung gian tế bào NK.
Nguồn tham khảo:
[1] Statistics adapted from the American Cancer Society’s publication, Cancer Facts & Figures 2023; the ACS website; the CBTRUS Statistical Report: Primary Brain and Other Central Nervous System Tumors Diagnosed in the United States in 2015-2019, published October 2022; the International Agency for Research on Cancer website; and the National Cancer Institute website. (All sources accessed February 2023.)
[2] WONG, Eric T.; WU, Julian K.; WEN, Patrick Y. Overview of the clinical features and diagnosis of brain tumors in adults. U: UpToDate, Loeffler JS, Wen PJ. UpToDate [Internet], 2020.
[3] FARES, Jawad, et al. Advances in NK cell therapy for brain tumors. npj Precision Oncology, 2023, 7.1: 17.
[4] YANG, Isaac, et al. The role of microglia in central nervous system immunity and glioma immunology. Journal of clinical neuroscience, 2010, 17.1: 6-10.
[5] LORGER, Mihaela. Tumor microenvironment in the brain. Cancers, 2012, 4.1: 218-243.
[6] SEDGWICK, Alexander James, et al. The role of NK cells and innate lymphoid cells in brain cancer. Frontiers in immunology, 2020, 11: 1549.
[7] FARES, Jawad; FARES, Mohamad Y.; FARES, Youssef. Natural killer cells in the brain tumor microenvironment: Defining a new era in neuro-oncology. Surgical neurology international, 2019, 10.
[8] BÖTTCHER, Jan P., et al. NK cells stimulate recruitment of cDC1 into the tumor microenvironment promoting cancer immune control. Cell, 2018, 172.5: 1022-1037. e14.
[9] FADUL, Camilo E., et al. Immune modulation effects of concomitant temozolomide and radiation therapy on peripheral blood mononuclear cells in patients with glioblastoma multiforme. Neuro-oncology, 2011, 13.4: 393-400.
[10] CASTRICONI, Roberta, et al. NK cells recognize and kill human glioblastoma cells with stem cell-like properties. The Journal of Immunology, 2009, 182.6: 3530-3539.
[11] ISHIKAWA, Eiichi, et al. Autologous natural killer cell therapy for human recurrent malignant glioma. Anticancer research, 2004, 24.3B: 1861-1871.
[12] BAGGIO, Letícia, et al. Natural killer cell adoptive immunotherapy: Coming of age. Clinical Immunology, 2017, 177: 3-11.