MSC-CM và tiềm năng điều trị tình trạng ung thư gan, viêm gan
Tỷ lệ mắc ung thư gan trên toàn thế giới đã được đề cập từ cơ sở dữ liệu GLOBOCAN 2020, bao gồm 185 quốc gia với số liệu trên 100.000 người/năm đã được tính toán. Vào năm 2020, ước tính có khoảng 905.700 người được chẩn đoán mắc bệnh và 830.200 người chết vì ung thư gan trên toàn cầu [1, 2]. Ung thư gan là một trong ba nguyên nhân hàng đầu gây tử vong do ung thư ở 46 quốc gia và nằm trong số năm nguyên nhân gây tử vong do ung thư ở 90 quốc gia [3]. Tỷ lệ mắc và tử vong ở nam cao hơn nữ ở tất cả các khu vực trên thế giới. Số ca ung thư gan mới mỗi năm được dự đoán sẽ tăng 55,0% từ năm 2020 đến năm 2040, với khả năng có 1,4 triệu người được chẩn đoán vào năm 2040. Dự đoán 1,3 triệu người có thể chết vì ung thư gan vào năm 2040 (cao hơn 56,4% so với năm 2020) [2]. Gánh nặng ung thư gan là khá phổ biến trên toàn thế giới. Ung thư gan do một số nguyên nhân có thể ngăn ngừa được nếu các nỗ lực kiểm soát được ưu tiên và sự gia tăng dự đoán trong các trường hợp có thể làm tăng nhu cầu về nguồn lực để quản lý chăm sóc bệnh nhân ung thư gan và ảnh hưởng tới chất lượng cuộc sống.
TẢI FILE PDF TẠI ĐÂY: MSC-CM và tiềm năng điều trị tình trạng ung thư gan, viêm gan – PDF
Phương pháp phổ biến của điều trị bệnh gan
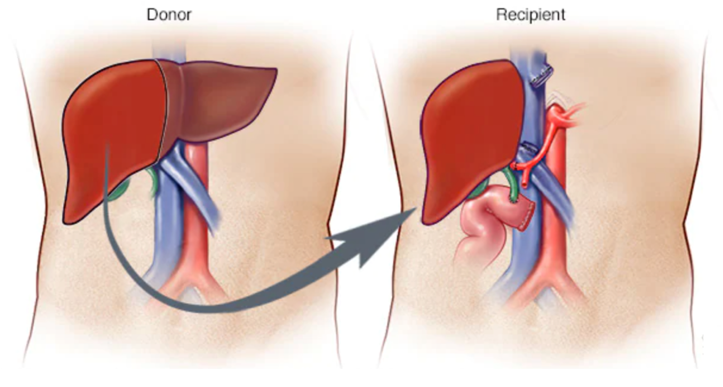
Một trong những liệu pháp điều trị hiệu quả nhất cho bệnh nhân suy gan cấp (ALF) là ghép gan, đây được coi như là một phương pháp tiêu chuẩn để điều trị cho các bệnh nhân này (Hình 1). Phương pháp này trải qua quá trình phẫu thuật để thay thế gan bị bệnh bằng gan khoẻ mạnh từ người hiến [4]. Tuy nhiên, do sự thiếu hụt gan của người hiến, chi phí thực hiện phẫu thuật và đặc biệt là những rào cản liên quan đến hệ miễn dịch ảnh hưởng rất nhiều đến bệnh nhân sau ghép gan [5]. Khoản chi phí lớn của ghép gan được báo cáo, khoảng 10 năm về trước ước tính chi phí trung bình của một ca ghép gan ở Hoa Kỳ là 163.438 USD Mỹ so với hiện nay chi phí ngày càng tăng và sự đoán khoảng 878,400 USD [6]. Đặc điểm của bệnh nhân, đặc điểm của bệnh, chất lượng của bệnh viện và đội ngũ y bác sĩ cấp dịch vụ chăm sóc sức khỏe và phương pháp phẫu thuật khác nhau dẫn đến sự khác biệt về chi phí. Gần đây, các nhà khoa học chỉ ra rằng việc ghép MSC cũng là một liệu pháp hứa hẹn trong điều trị các tổn thương về gan. Tuy nhiên, vẫn còn những mối lo ngại về việc sử dụng MSC trong điều trị cũng như những cơ chế điều trị bệnh gan chưa rõ ràng [7].
Hình 1: Bệnh nhân được nhận thuỳ phải từ gan của người hiến
Tiềm năng của MSC-CM trong việc điều trị bệnh gan
Tế bào gốc trung mô (mesenchymal stem cells – MSC) đang nổi lên như một đối tượng tiềm năng trong điều trị nhiều bệnh lý khác nhau do tiềm năng tái tạo của chúng. Tuy nhiên, cơ chế điều trị bệnh và rủi ro có thể mắc phải khi sử dụng MSC vẫn còn đang là một thách thức lớn đối với các nghiên cứu. Để hạn chế những rủi ro khi sử dụng MSC trong điều trị bệnh, liệu pháp sử dụng môi trường điều hoà (conditioned media) nuôi MSC có chứa hệ tiết (secretome) từ tế bào gốc được đề xuất như một liệu pháp không sử dụng tế bào (cell-free therapy) để điều trị lý khác nhau cũng như là các tổn thương về gan như suy gan, xơ gan [8]. Có rất nhiều nguyên nhân dẫn đến tình sạng suy gan như virus viêm gan A, viêm gan B, viêm gan C hay do xơ gan kéo dài; trong đó, sự phát triển của suy gan cấp tính trên nền mạn tính (ACLF) là nguyên nhân quan trọng nhất gây tử vọng ở bệnh nhân. Hơn nữa, ACLF đặc trưng bởi sự gia tăng viêm toàn thân cùng với việc giảm khả năng tái tạo tế bào gan dẫn đến suy đa tạng [9]. Do vậy, CM của MSC bao gồm các yếu tố điều hoà miễn dịch và kích thích tăng sinh tế bào gan có thể làm cải thiện tình trạng gan của bệnh nhân [10].
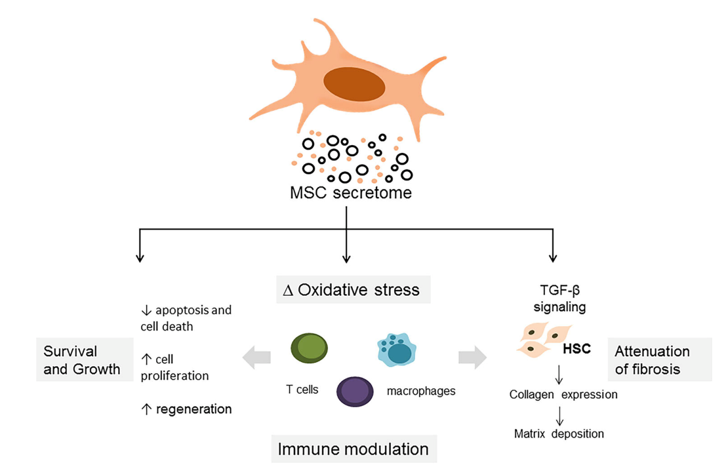
Môi trường điều hoà (conditioned media) của MSC trong nuôi cấy in vitro có chứa chủ yếu là các thành phần hệ tiết, gồm có là các protein hoà tan và thể tiết ngoại bào (Extracellular vesicles – EVs). Chúng có các đặc tính tái tạo thông qua hiệu quả điều hoà hệ miễn dịch, cải thiện tổn thương và giảm xơ hoá ở gan (Hình 2). CM có chứa các protein hoà tan như cytokine hay chemokine được tiết từ MSC có khả năng tác động trực tiếp hoặc gián tiếp lên các tế bào miễn dịch ở mô tổn thương. Cụ thể, các yếu tố sinh trưởng và cytokine trong hệ tiết như yếu tố chuyển đổi tăng trưởng beta (TGF-β), yếu tố tăng trưởng tế bào gan (HGF), interleukin10 (IL-10), postagladin E2 (PGE2) [11] có thể điều hoà tín hiệu, kích thích tế bào gan tăng sinh và giảm xơ hoá. Ngoài các protein hoà tan, thể tiết ngoại bào (EVs) trong CM cũng có khả năng điều hoà miễn dịch thông qua việc kích hoạt các con đường truyền tín hiệu khác nhau (STAT3, Bcl2) [12]. Trong cả 2 mô hình in vitro và in vivo, CM từ MSC có nguồn gốc từ dây rốn cho thấy khả năng giảm lượng tế bào chết tự nhiên trong mô hình suy gan, đồng thời làm giảm chỉ số aspartate aminotransferase (AST), alanine aminotransferase (ALT) trong huyết thanh [13].
Hình 2: Cơ chế điều trị bệnh của hệ tiết từ MSC [14]
Về tiềm năng phát triển trong tương lai, CM có chứa hệ chất tiết từ MSC là một lựa chọn mới và hấp dẫn cho các ứng dụng điều trị như là một liệu pháp tái tạo cho các bệnh về tổn thương gan, xơ gan hay suy gan. Mặc dù hiện nay chưa có bất kì thử nghiệm lâm sàng nào sử dụng CM từ MSC trong điều trị bệnh lý gan; tuy nhiên, những dữ liệu và kết quả tích cực thu được từ nghiên cứu in vitro và in vivo tiền lâm sàng cho thấy rằng việc nghiên cứu, đánh giá và sử dụng chúng trên lâm sàng là điều rất cần thiết.
Tài liệu tham khảo:
1.Sung H, Ferlay J, Siegel RL, Laversanne M, Soerjomataram I, Jemal A, Bray F: Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin 2021, 71(3):209-249.
2.Rumgay H, Arnold M, Ferlay J, Lesi O, Cabasag CJ, Vignat J, Laversanne M, McGlynn KA, Soerjomataram I: Global burden of primary liver cancer in 2020 and predictions to 2040. J Hepatol 2022, 77(6):1598-1606.
3.Arnold M, Abnet CC, Neale RE, Vignat J, Giovannucci EL, McGlynn KA, Bray F: Global Burden of 5 Major Types of Gastrointestinal Cancer. Gastroenterology 2020, 159(1):335-349 e315.
4.Shi M, Zhang Z, Xu R, Lin H, Fu J, Zou Z, Zhang A, Shi J, Chen L, Lv SJSctm: Human mesenchymal stem cell transfusion is safe and improves liver function in acute-on-chronic liver failure patients. 2012, 1(10):725-731.
5.Lee C-W, Chen Y-F, Wu H-H, Lee OKJG: Historical perspectives and advances in mesenchymal stem cell research for the treatment of liver diseases. 2018, 154(1):46-56.
6.van der Hilst CS, Ijtsma AJ, Slooff MJ, Tenvergert EM: Cost of liver transplantation: a systematic review and meta-analysis comparing the United States with other OECD countries. Med Care Res Rev 2009, 66(1):3-22.
7.Musiał-Wysocka A, Kot M, Majka MJCt: The pros and cons of mesenchymal stem cell-based therapies. 2019, 28(7):801-812.
8.Hu C, Zhao L, Zhang L, Bao Q, Li LJSCR, Therapy: Mesenchymal stem cell-based cell-free strategies: safe and effective treatments for liver injury. 2020, 11(1):1-12.
9.Khanam A, Kottilil SJFiM: Acute-on-chronic liver failure: pathophysiological mechanisms and management. 2021, 8:752875.
10.Alfaifi M, Eom YW, Newsome PN, Baik SKJJoh: Mesenchymal stromal cell therapy for liver diseases. 2018, 68(6):1272-1285.
11.Parekkadan B, van Poll D, Megeed Z, Kobayashi N, Tilles AW, Berthiaume F, Yarmush MLJB, communications br: Immunomodulation of activated hepatic stellate cells by mesenchymal stem cells. 2007, 363(2):247-252.
12. Haga S, Terui K, Zhang HQ, Enosawa S, Ogawa W, Inoue H, Okuyama T, Takeda K, Akira S, Ogino TJTJoci: Stat3 protects against Fas-induced liver injury by redox-dependent and-independent mechanisms. 2003, 112(7):989-998.
13.Van Poll D, Parekkadan B, Cho CH, Berthiaume F, Nahmias Y, Tilles AW, Yarmush MLJH: Mesenchymal stem cell–derived molecules directly modulate hepatocellular death and regeneration in vitro and in vivo. 2008, 47(5):1634-1643.
14. Driscoll J, Patel TJJog: The mesenchymal stem cell secretome as an acellular regenerative therapy for liver disease. 2019, 54:763-773.