Tế bào gốc màng ối trong Y học tái tạo: Những ứng dụng trong tương lai
Tiềm năng sinh học của tế bào gốc màng ối AMSC đã và đang được đẩy mạnh nghiên cứu, mở ra triển vọng điều trị cho nhiều bệnh lý khác, không chỉ liên quan đến thần kinh.
Đột quỵ và chấn thương sọ não
Một trong những ứng dụng có thể có của tế bào gốc màng ối AMSC trong điều trị đột quỵ và chấn thương sọ não (TBI) là thông qua miếng dán dưới màng cứng. Phương pháp này bao gồm việc đặt một miếng dán từ màng ối trực tiếp lên não, khai thác các đặc tính điều trị của nó và cung cấp mảnh ghép không gây độc tố do khả năng biệt hóa và tích hợp vào mô não.
Các tế bào gốc từ miếng dán sẽ tạo điều kiện thuận lợi cho sự di chuyển của các tế bào đa năng, cả được cấy ghép và tạo ra trong não, đến vị trí bị thương. Các kết nối này, hoặc các tế bào sinh học, đã được quan sát thấy trong các nghiên cứu trước đây sử dụng các tế bào trung mô đệm có nguồn gốc từ tủy xương của con người để điều trị chấn thương sọ não trên mô hình chuột.
Khả năng hình thành các tế bào sinh học và biệt hóa thành các tế bào tiền thân thần kinh làm cho miếng dán màng ối trở thành một liệu pháp lý tưởng không chỉ để điều chỉnh chứng viêm mà còn để thúc đẩy quá trình tái tạo thần kinh.
Mặc dù chưa có bất kỳ mô hình thử nghiệm nào về sự hình thành biobridge (cầu sinh học) trong đột quỵ, nhưng người ta đã đưa ra giả thuyết rằng các tế bào gốc có khả năng hoạt động theo cách tương tự, cho phép các tế bào gốc thần kinh di chuyển về khu vực cốt lõi của tổn thương đột quỵ và thiếu máu cục bộ.
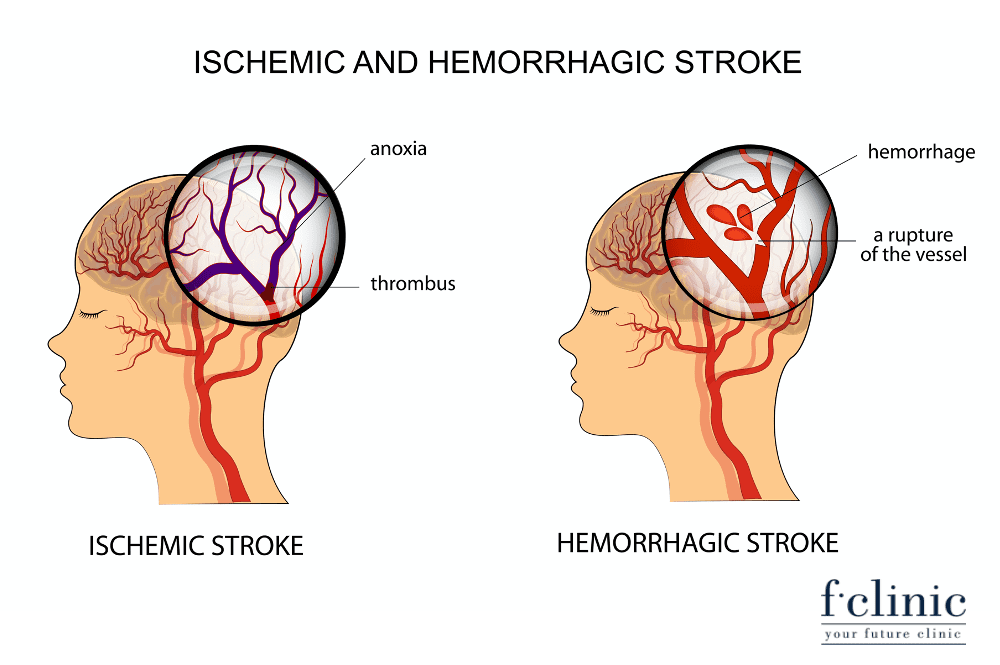
Có 2 loại đột quỵ não chính: đột quỵ nhồi máu não (ischemic stroke – do tắc mạch) hoặc đột quỵ chảy máu não (hemorrhagic stroke – do vỡ mạch)
Các rối loạn thần kinh do viêm
Khả năng điều chỉnh tình trạng viêm làm cho các tế bào biểu mô màng ối – hAECs hữu ích trong việc điều trị các rối loạn thần kinh do viêm. Các yếu tố điều hòa miễn dịch được tiết ra bởi tế bào biểu mô màng ối hAEC, chẳng hạn như prostaglandin E-2 (PGE2), điều chỉnh phản ứng miễn dịch, ngăn chặn tình trạng viêm và do đó làm giảm các tác dụng phụ của nó.
Một đặc điểm thú vị khác của những tế bào này là sự biểu hiện của chúng với kháng nguyên bạch cầu người G (HLA-G), cho phép chúng trốn tránh hệ thống miễn dịch và gây ra quá trình apoptosis (sự chết tế bào) trong các tế bào miễn dịch.
Hiệu ứng này cũng đã được quan sát thấy trên các mô hình chuột đa xơ cứng (MS), nơi alpha-fetoprotein ức chế viêm và bên ngoài thần kinh trung ương trong các mô hình tổn thương phổi, trong đó các tế bào biểu mô màng ối hAEC ức chế sự bài tiết các cytokine tiền viêm và tăng tiết các cytokine chống viêm.
Việc sửa đổi hAEC để tạo ra các cytokine chống viêm và chemokine in vivo (thí nghiệm trên động vật) sẽ cho phép định lượng và đánh giá việc sử dụng chúng trên lâm sàng trong các bệnh liên quan đến viêm. Ngoài ra, việc sử dụng các yếu tố này cùng với liệu pháp tế bào gốc màng ối AMSC sẽ phát huy tác dụng chống viêm của chúng, mang lại một phương pháp điều trị hiệu quả hơn.
Xem thêm:
Ứng dụng của tế bào gốc màng ối trong điều trị rối loạn thần kinh
Sử dụng tế bào gốc màng ối trong điều trị các bệnh không liên quan đến hệ thần kinh trung ương
Điều trị sau Covid bằng liệu pháp tế bào gốc để sửa chữa các tổn thương cơ quan
Mảnh ghép từ màng ối
Cả tế bào biểu mô màng ối hAEC và mảnh ghép từ màng ối đều có các đặc tính điều hòa miễn dịch giống nhau, đã được mô tả ở trên. Các miếng dán màng ối đã được chứng minh là thúc đẩy sự hình thành vi môi trường có lợi cho việc chữa lành vết thương của các tế bào vật chủ, cho phép chữa lành vết thương tốt hơn.
Một ưu điểm khác của các miếng dán màng ối ở người là tương đối dễ chuẩn bị, chỉ yêu cầu tách amnion khỏi màng đệm mà không cần nuôi cấy hoặc phân lập.
Tuy nhiên, tác dụng điều trị của chúng bắt nguồn từ việc điều chỉnh vi môi trường tổn thương, chứ không phải là sự khác biệt của các tế bào gốc màng ối AMSC. Mặt khác, tế bào biểu mô màng ối hAECs đã thể hiện khả năng biệt hóa thành tế bào gốc thần kinh cũng như điều chỉnh phản ứng viêm, làm tăng trường hoạt động tiềm năng của chúng.
Mảnh ghép từ màng ối
Các thử nghiệm được tiến hành với các tế bào giống tế bào gốc thần kinh thu được từ tế bào biểu mô màng ối hAEC đã biệt hóa đã cho thấy sự gia tăng bài tiết các yếu tố dinh dưỡng thần kinh. Do đó, hAEC nên được nuôi cấy trong môi trường thuận lợi cho sự phân biệt để khai thác đầy đủ tiềm năng điều trị của chúng.
Việc cấy ghép các mô từ loài này sang loài khác, được gọi là cấy ghép xenografting (ghép dị lai), đã cho thấy nhiều hứa hẹn trong việc điều trị nhiều loại bệnh. Tuy nhiên, một loạt các biến chứng miễn dịch phát sinh do hệ thống miễn dịch của vật chủ từ chối các mảnh ghép. Sự đào thải này dẫn đến việc sản xuất các kháng thể xenoreactive, gây viêm hệ thống và kích hoạt hệ thống bổ thể.
Mặc dù nhiều kỹ thuật dung nạp đã được thử nghiệm, chẳng hạn như giải mẫn cảm, nhưng vẫn không cải thiện được tỷ lệ đào thải.
Một lựa chọn đã hoạt động trong các nghiên cứu trước đó là áp dụng protein chống viêm tuần hoàn alpha-1-antitrypsin (ATT), cùng với liệu pháp kháng CD4/ CD8, bảo vệ mảnh ghép khỏi bị viêm và do đó, không bị đào thải. Cơ chế này mở ra khả năng sử dụng tế bào gốc màng ối người hASC để ngăn chặn đào thải mảnh ghép bằng cách điều chỉnh phản ứng miễn dịch. Bằng cách cấy ghép hASC cùng lúc với mảnh ghép, tỷ lệ đào thải của chúng sẽ giảm xuống.
Allografts, hoặc cấy ghép mô từ cá thể này sang cá thể khác cùng loài, không có khả năng miễn dịch với sự đào thải, với khả năng trở thành mục tiêu của các cơ quan phòng thủ của vật chủ là rất cao. Trở ngại đầu tiên mà allografts gặp phải là phản ứng miễn dịch bẩm sinh của vật chủ, không đặc hiệu. Sau đó, allografts đối mặt với phản ứng miễn dịch cụ thể, qua trung gian của các tế bào T được thiết kế đặc biệt để nhận ra các chất gây dị ứng. Một số nghiên cứu đã sử dụng tế bào gốc màng ối AMSC kết hợp với allografts để điều chỉnh phản ứng miễn dịch đối với mảnh ghép, giảm nhu cầu điều trị ức chế miễn dịch và được vật chủ chấp nhận.
Viêm hệ thần kinh ngoại vi
Tình trạng viêm đặc trưng cho rối loạn thần kinh trung ương không chỉ xuất hiện ở thần kinh trung ương mà còn lan đến hệ thần kinh ngoại vi (PNS). Sự tham gia này của PNS trong phản ứng viêm sau chấn thương tạo ra một loạt các cơ hội chẩn đoán và điều trị thú vị như khả năng điều trị viêm hệ thần kinh ngoại vi PNS bằng tế bào gốc màng ối AMSC.
Trong số các cơ quan ngoại vi có biểu hiện viêm sau đột quỵ là lá lách, nơi có thể dễ dàng bị các tế bào gốc nhắm mục tiêu. Điều này sẽ được thực hiện bằng cách cấy ghép toàn thân các tế bào gốc hướng đặc biệt đến lá lách hoặc bằng cách cấy ghép các tế bào vào cơ quan. Khi tế bào gốc màng ối AMSC đến lá lách, các đặc tính chống viêm của chúng sẽ làm giảm bớt tình trạng viêm ngoại vi.
Các ứng dụng khác
Mặc dù có nhiều tế bào đa năng có nguồn gốc từ các mô của thai kỳ (chẳng hạn như máu dây rốn, thạch Wharton và nước ối), nhưng tế bào gốc màng ối AMSC là loại tế bào duy nhất có thể được sử dụng mà không cần nuôi cấy trước đó.
Vì tế bào gốc biểu mô màng ối người hAECs đã cho thấy tiềm năng biệt hóa in vitro (trong phạm vi phòng thí nghiệm) rất đa dạng, chúng có thể hữu ích trong nhiều loại bệnh. Các nghiên cứu đã chứng minh khả năng biệt hóa của chúng thành một số mô bao gồm mô mỡ, tế bào cơ tim, tuyến tụy, gan, thần kinh, tạo xương và chondrogenic.
Do đó, tế bào gốc màng ối AMSC có thể được thu hoạch khi mới sinh và hướng đến các phương pháp điều trị cụ thể cho những người có nguy cơ của các bệnh đang phát triển. Thông qua xét nghiệm di truyền, những cá nhân có nguy cơ phát triển bệnh ở tuổi trưởng thành có thể bắt đầu bằng liệu pháp tế bào gốc màng ối AMSC dự phòng, làm chậm hoặc thậm chí ngừng phát triển các rối loạn này.
Ngân hàng lưu trữ tế bào gốc quốc tế Cryoviva là ngân hàng đầu tiên tại Việt Nam cung cấp dịch vụ lưu trữ cho 04+ loại tế bào từ cuống rốn trẻ sơ sinh: Máu cuống rốn (HSC), mô cuống rốn (MSC, EpSC) và màng bánh nhau – màng ối (AMSC).
ĐẶT LỊCH TƯ VẤN ĐIỀU TRỊ TẠI NƯỚC NGOÀI
Điện thoại0937 53 45 45
info.fclinic@gmail.com
